全文速览
本工作设计合成Co、V共掺杂的NiS2催化剂用于电催化尿素氧化(UOR),最终实现高效的阴极析氢。深入剖析了Ni,Co,V三元素之间的作用和催化机理。发现Ni元素作为主催化活性位点,Co元素加速碳质中间产物氧化以提高催化剂的稳定性,V元素特殊轨道属性提升Ni和Co的催化活性。通过原位电化学拉曼光谱以及原位电化学质谱同位素示踪实验证明金属硫化物催化下UOR符合分子内N-N偶联机制,并采用DFT计算为三元催化剂的高活性反应路径提供了理论支持。
背景介绍
面对全球能源环境危机,寻找清洁能源至关重要。利用电化学水裂解制氢气获得了广泛关注。为了克服阳极氧气析出反应(OER)滞缓的动力限制,以有机小分子阳极氧化替代OER颇具前途。尿素氧化(UOR)的理论电位仅0.37 V(vs.RHE),同时尿素来源广泛,包括生活和工业废水,以UOR替代OER有望实现在净化尿素废水的同时实现高效产氢。然而UOR这样一个复杂的6电子转移过程,要想实现其高效彻底的催化氧化绝非易事。目前UOR催化剂的研究主要围绕Ni基,包括氧化镍,氢氧化镍,硫化镍等,其中基于硫化物的UOR的反应机理尚不明确。因此,我们选择NiS2为主体研究对象,从活性和稳定性两个角度入手,启动双掺杂策略,制备了Co,V共掺杂的NiS2电催化剂用于电催化尿素氧化,并深入探究该催化剂催化下的UOR机理。利用XPS光谱,电化学原位拉曼光谱,电化学原位质谱同位素示踪实验以及DFT计算为材料内部的协同作用以及UOR反应路径带来了实验和理论支持,这为金属硫化物催化下的UOR研究提供了一些研究方法和新思路。
本文亮点
1、该工作从活性和稳定性两个角度入手,利用Co和V作为掺杂剂协同提高了NiS2电催化剂在UOR中的表现。利用CO抗中毒实验以及稳定性测试成功证明Co元素可以加速尿素氧化过程中产生的碳质中间产物(例如 CO)的氧化,防止活性位点中毒,提高稳定性。
2、利用XPS光谱以及电化学测试证明3d空轨道全空的V元素接收来自Ni和Co元素的电子,进而调控Ni、Co的催化活性。
3、利用原位电化学拉曼光谱成功证明HN-CO-NH以及CO中间体的存在,原位电化学质谱同位素示踪实验证明在镍基硫化物催化下,尿素氧化产物N2是来源于尿素分子内的N-N偶联。
图文解析
A. 材料形貌
材料制备过程如图1a所示,我们以相应的金属盐和均苯三甲酸以及PVP为原料,首先利用水热法得到金属元素均匀分布的配合物前体,然后以硫代乙酰胺(TAA)为硫源,再次利用水热法得到尺寸为200 nm左右的Co,V共掺杂的NiS2电催化剂。相比于直接用金属盐和TAA反应得到的产物,该方法得到的催化剂尺寸更小,比表面积更大,有利于提高材料的利用率。图1b的SEM图像以及图1c的TEM图像均表明所制备材料NCVS-3是200nm左右,大小均匀的颗粒。HRTEM(图1d)以及选区电子衍射(图1e)结果表明NiS2(200)晶面是主要暴露晶面。相比于纯NiS2,NCVS-3的晶格间距发生了一定程度的收缩,这可能是因为Co,V杂原子的引入。EDS元素mapping图进一步证明了Ni,Co,V元素的存在和均匀分布。

Figure 1. (a) The fabrication process of NCS, NVS and NCVS; (b) SEM, (c) TEM, (d) HRTEM image and (e) SAED of NCVS-3; (f) SEM image of NCVS-3 and corresponding elemental mappings of Ni, Co,V, S.
B. 电子结构 为了证明材料内部金属元素之间的电荷转移,我们开展了一系列的XPS测试。如图2a所示,Ni 2p3/2光谱显示Co或者V元素的引入使其结合能发生明显的正向移动,表明Ni上电子减少,Co 2p3/2结果表明V元素的引入使Co上电子减少(图2b)。作为掺杂剂引入NiS2的V元素的氧化态明显低于单纯硫化钒。更重要的是,如图2c所示,相比于NVS-1材料,NCVS-3中V的结合能负移程度更大,表明V元素不仅可以调节Ni的电子结构,也可以调节Co。我们尝试以扩展的超交换作用理解材料内部的电子转移现象,如图2f所示, S-S 键作为电子传输桥梁,在 Ni-S-S-V 模型中,具有完全占据的 π 对称d轨道 (t2g)的 Ni2+ 倾向于通过 S22-将电子转移到具有低占据 t2g d轨道的V 和Co。Co-S-S-V 中的电子传输类似,电子倾向于从Co转移到V。
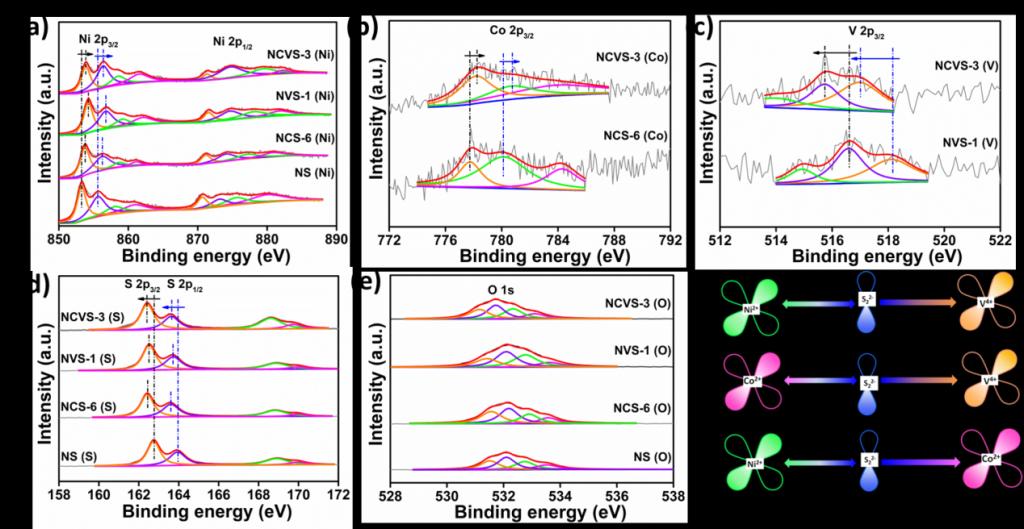
Figure 2. High-resolution XPS spectra of (a) Ni 2p of NS, NCS-6, NVS-1 and NCVS-3; (b) Co 2p3/2 of NCS-6 and NCVS-3; (c) V 2p3/2 of NVS-1 and NCVS-3; (d) S 2p and (e)O 1s of NS, NCS-6, NVS-1 and NCVS-3; (f) Schematic representations of the electronic coupling among Ni, Co, and V in NCVS-3.
C.电化学测试 如图3a所示,线性扫描伏安法结果表明最优样品NCVS-3仅需要1.35 V (vs. RHE)就可以达到10 mA cm-2,在1.5 V(vs. RHE) 电位可以达到83 mA cm-2。催化剂的稳定性是判断催化性能的重要指标。图3b 显示了 NS、NCS-6、NVS-1 和 NCVS-3 10 小时的 UOR 计时电流曲线,电流密度j 的衰减率为 25.90% (NVS-1)、25.09% (NS)、10.49% (NCS-6)和 6.19% (NCVS-3)(图 3c)。气相色谱 (GC) 用于探索NS、NCS-6、NVS-1 和 NCVS-3 的制氢能力,如图 3d 所示,在 1.8 V (vs. RHE) 电位下,NCVS-3 的产氢速率可以达到 143 L min-1 gcat-1。
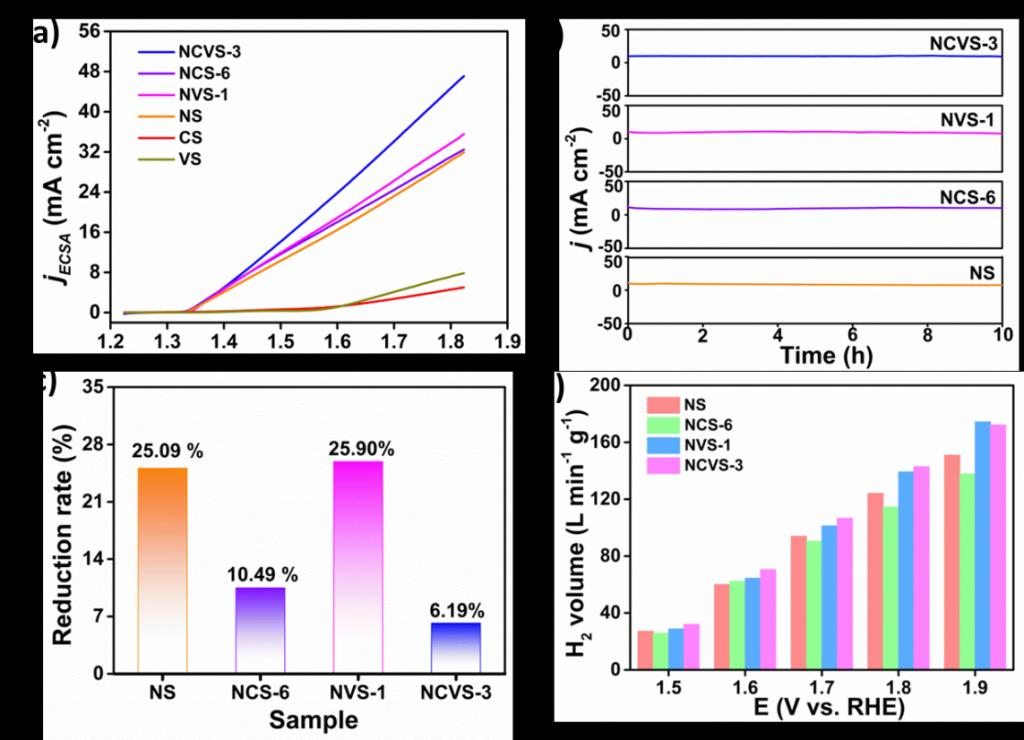
Figure 3. (a) LSV curves of NS,CS, VS and a series of optimal materials (NCS-6, NVS-1 and NCVS-3) in the electrolyte of 1 M KOH and 0.33 M urea at a scan rate of 5 mV s−1; (b)The time-dependent current density curves of NS, NCS-6, NVS-1 and NCVS-3 at the potential of 1.36 V (vs. RHE) and (c) corresponding calculated current density decay rate; (d) Hydrogen production rate of NS, NCS-6, NVS-1 and NCVS-3 atdifferent potential in 1 M KOH and 0.33 M urea.
D. 理论分析 为了进一步加深对催化过程的理解,我们开展了原位实验和理论计算。NCVS-3的电化学原位电化学拉曼光谱结果如图4a所示,随着电位的升高,474 cm-1处隶属于NiS2的峰仍然存在,表明材料结构基本稳定。当电位高于 1.5 V (vs. RHE)时,1314 cm-1 处出现小峰,表明 HN-CO-NH 结构出现,因此可以推测尿素分子中H原子的脱除顺序是对称脱除。CO关键中间体也在2114 cm-1 处被发现。为了进一步探究硫化物催化下的UOR路径,我们开展了电化学原位质谱同位素示踪实验。如图 4b 所示,当电解液中仅含有 CO(14NH2)2+KOH时,14N2 信号随着电位的开关而发生明显的变化,而14N15N 和 15N2 的信号基本无变化。当电解液同时含有CO(14NH2)2+CO(15NH2)2+KOH时,14N2 和15N2信号随电位发生明显变化,14N15N信号基本无变化 (图4c),这一结果有力地证明了产物N2来源于尿素分子间 N-N 偶联。基于以上的原位测试结果,我们给出了Co,V共掺杂NiS2催化下的UOR可能路径,如图4d所示,V元素主要用于调节Ni和Co的催化活性,不参与整个催化过程,而Ni, Co元素作为协同催化位点,共同削弱C-N键,最终将尿素分解成N2和CO2。最后, DFT 计算被用来研究 Ni、Co 和 V 元素在 UOR 催化路径中的作用,反应路径的自由能揭示了三元协同系统的优越性(图4e)。由于V的引入降低了Ni和Co的电子密度和NH的能垒,NCVS(I→II)催化CO(NH)2形成CON2的自由能最低(3.68 eV)。C-N键断裂和N-N耦合(II→III)后,V和Co共存促进了CO碎片氧化形成HO-CO(III→IV),在NCVS催化下需要的自由能最低。随后,HO-CO碎片在碱性溶液中转化为 CO32-(IV→V)。
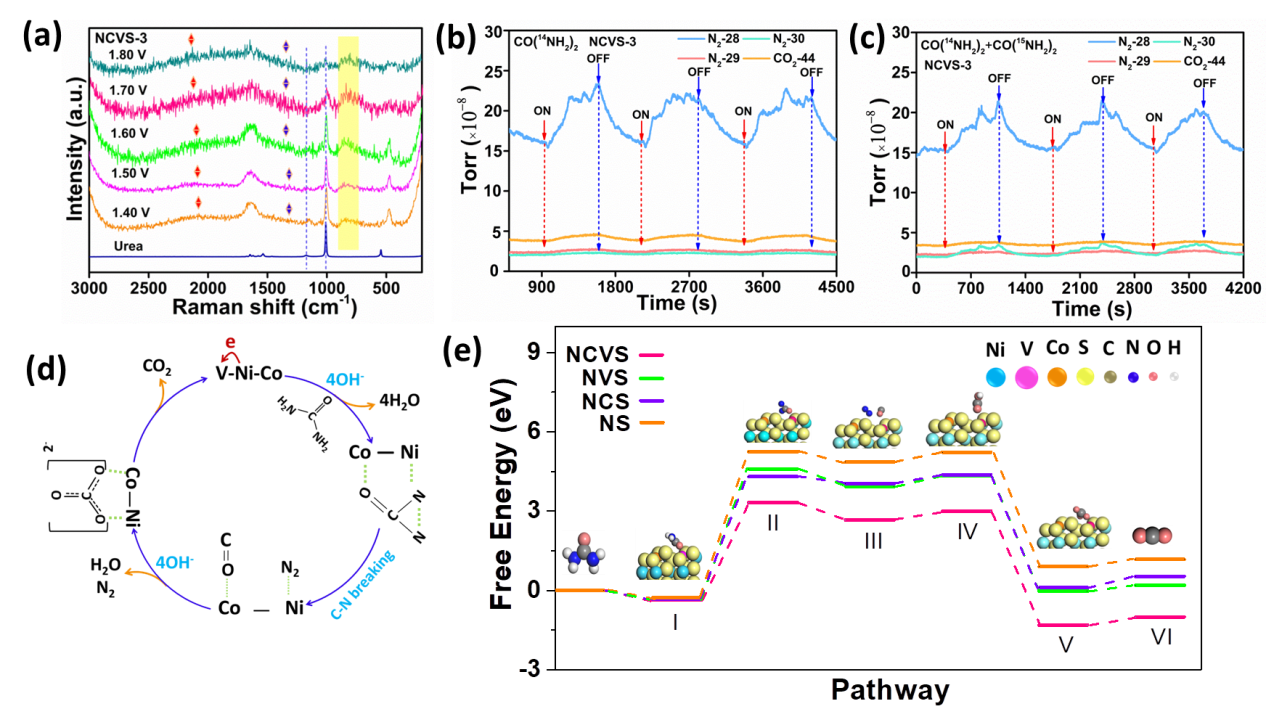
Figure 4. (a) In-situ electrochemistry Raman spectroscopy of UOR reaction catalyzed by NCVS-3 catalysts at a various potential from 1.40 V to 1.80 V (vs. RHE); In situ electrochemistry masss pectrometry isotope tracing experiment for periodic measurement of the UOR in 1 M KOH with (b) 0.33 M urea (CO(14NH2)2) and (c) 0.33 M urea (CO(14NH2)2 : CO(15NH2)2=4:1) under the catalysis of NCVS-3; (d) Possible UOR mechanism on the NCVS-3 electrode; (e) The Gibbs free energy profiles calculated at the standard conditions and the simplified surface structures of the various reaction species along the reaction pathways of UOR on the surface of NS, NCS, NVS and NCVS.
总结与展望
本文以金属配合物为前驱体,硫代乙酰胺为硫源,利用两步水热法得到Co,V共掺杂的NiS2电催化剂用于电催化尿素氧化。Ni元素作为主要活性位点,Co元素用来提高材料稳定性,缓解催化剂中毒,具有大量空的3d轨道的V元素可以接收来自Ni和Co元素的电子,提高Ni和Co的活性,三种元素各司其职,最终在1.8 V (vs. RHE) 电位下H2生成速率达到143 L min-1 gcat-1,且稳定性良好。最重要的是,本文利用原位电化学拉曼光谱成功捕捉到催化过程中产生的中间体,原位电化学质谱同位素示踪实验结果证明在硫化物催化下,产物N2是来源于尿素分子内的N-N偶联,这对于理解催化路径是至关重要的。最后利用DFT计算,结合催化过程,为三元协同催化剂的高活性给出了合理解释。
心得与体会
科研不是一蹴而就的,从一个idea到一篇文章,过程往往是充满坎坷,在实验过程中我们会遇到各种各样意想不到的问题,面对实验结果,我们应该静下心来好好分析,问自己几个问题:这是我想要的结果吗?如果不是,问题可能出在哪里呢?有哪些解决办法?想好之后尽快落实到行动上,切勿纸上谈兵。同时,实验过程中要注意观察实验现象,不能反应做上就溜之大吉,等结束的时候才来看看,在整个过程中我们都要仔细观察,当出现某种不合常理的现象时及时记录并探究原因,也许创新的工作就是来源于这儿呢。最后就是要勤于思考,多看文献,了解同行做到什么程度了,多想该领域还存在哪些未解决的问题,多做一些新鲜的实验尝试,有条不紊地开展科研。路漫漫其修远兮,吾将上下而求索,希望每个科研人都可以取得丰硕成果。
论文链接: https://pubs.acs.org/doi/10.1021/acscatal.1c05190
来源:邃瞳科学云 https://mp.weixin.qq.com/s/_i8gaaL3Piij3MyyulVXKQ