研究背景
羟胺(NH₂OH)是一种关键的化工中间体,广泛用于尼龙-6、半导体、农药等领域。传统的羟胺制备方式依赖于氨的氧化还原过程,需高能耗且排放严重。电催化硝酸盐还原(ENRH)是一种绿色替代途径,但当前常用的活性氢(*H)来源存在两个难题:氢源不足导致亚硝酸盐积累,过量则易将羟胺过还原为氨。因此,开发“合适”的氢源成为该反应的关键瓶颈。
文章创新点
本文由天津大学于一夫教授团队提出以晶格氢替代表面活性氢(*H)作为氢源的新策略,实现高效羟胺合成:
● 创新引入Cu元素诱导Jahn-Teller效应,显著提高晶格氢数量;
● 构建Cu-MnO₂Hx电催化剂,晶格氢可控释放与补充,实现动态平衡;
● NH₂OH的法拉第效率高达91.1%,产率达396.6 mmol gcat −1 h −1,远超目前主流催化剂;
● 同位素追踪 + 理论计算明确晶格氢的“富集+缓冲”双重机制。
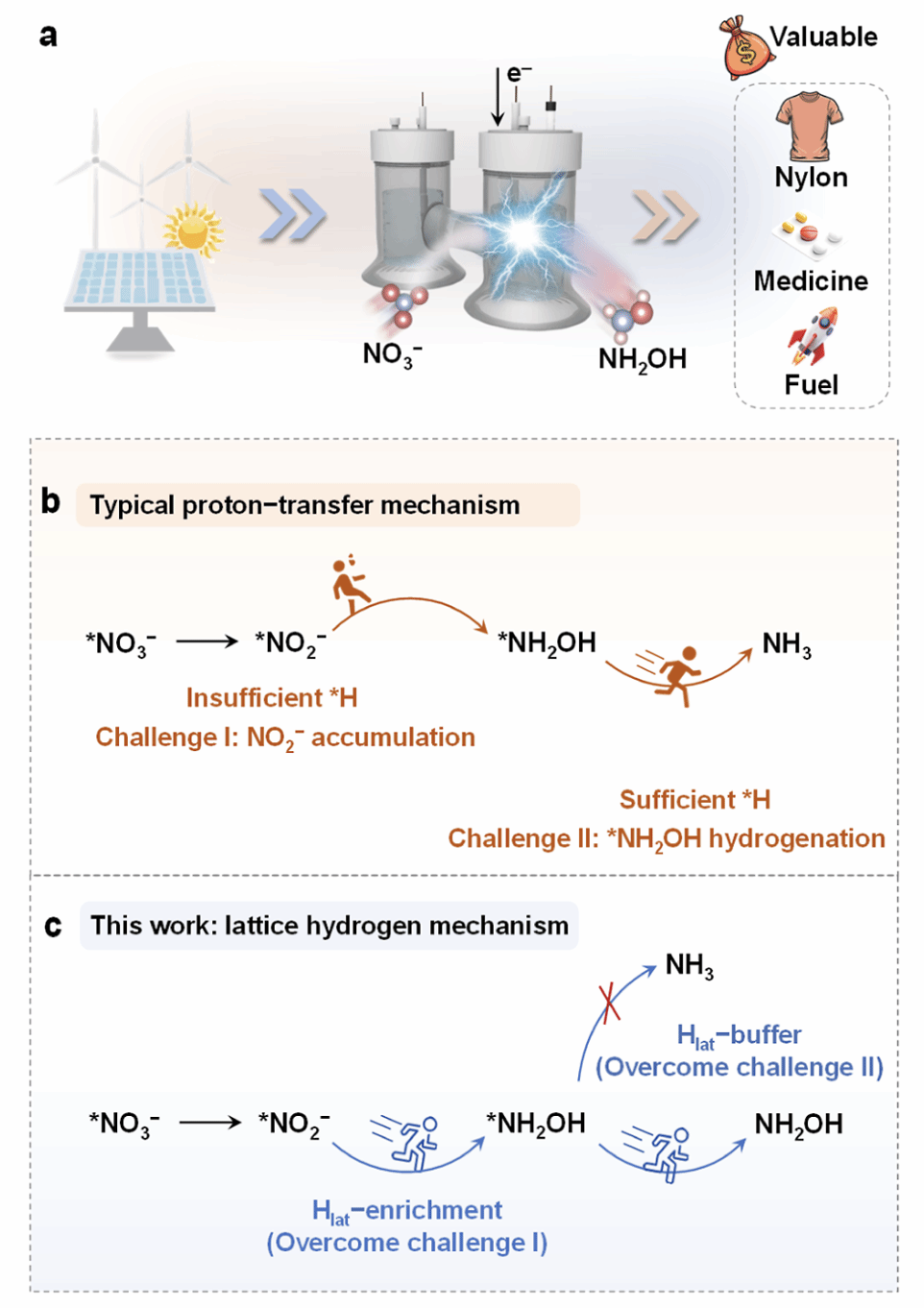
Figure 1:机制示意图
(a) 显示传统与本研究ENRH过程对比。
(b) 总结了使用*H的两个主要挑战。
(c) 提出了以晶格氢为氢源的新路径。
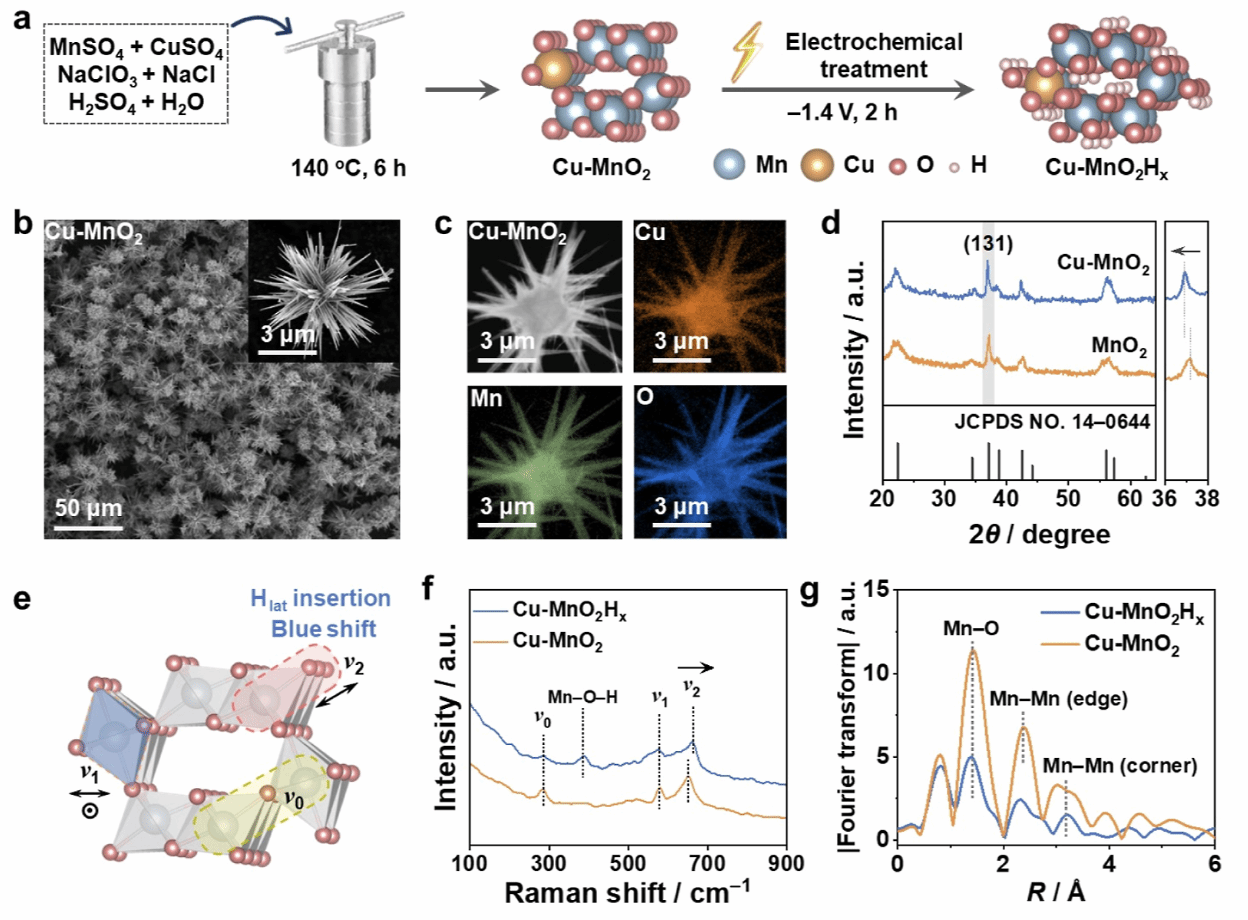
Figure 2:Cu-MnO₂Hx的合成与结构表征
SEM和EDS确认催化剂结构为海胆状、Cu元素分布均匀。
Raman光谱表明晶格氢的插入引起特征峰位移。
FT-EXAFS分析证实晶格中H的引入和MnO₆八面体畸变。
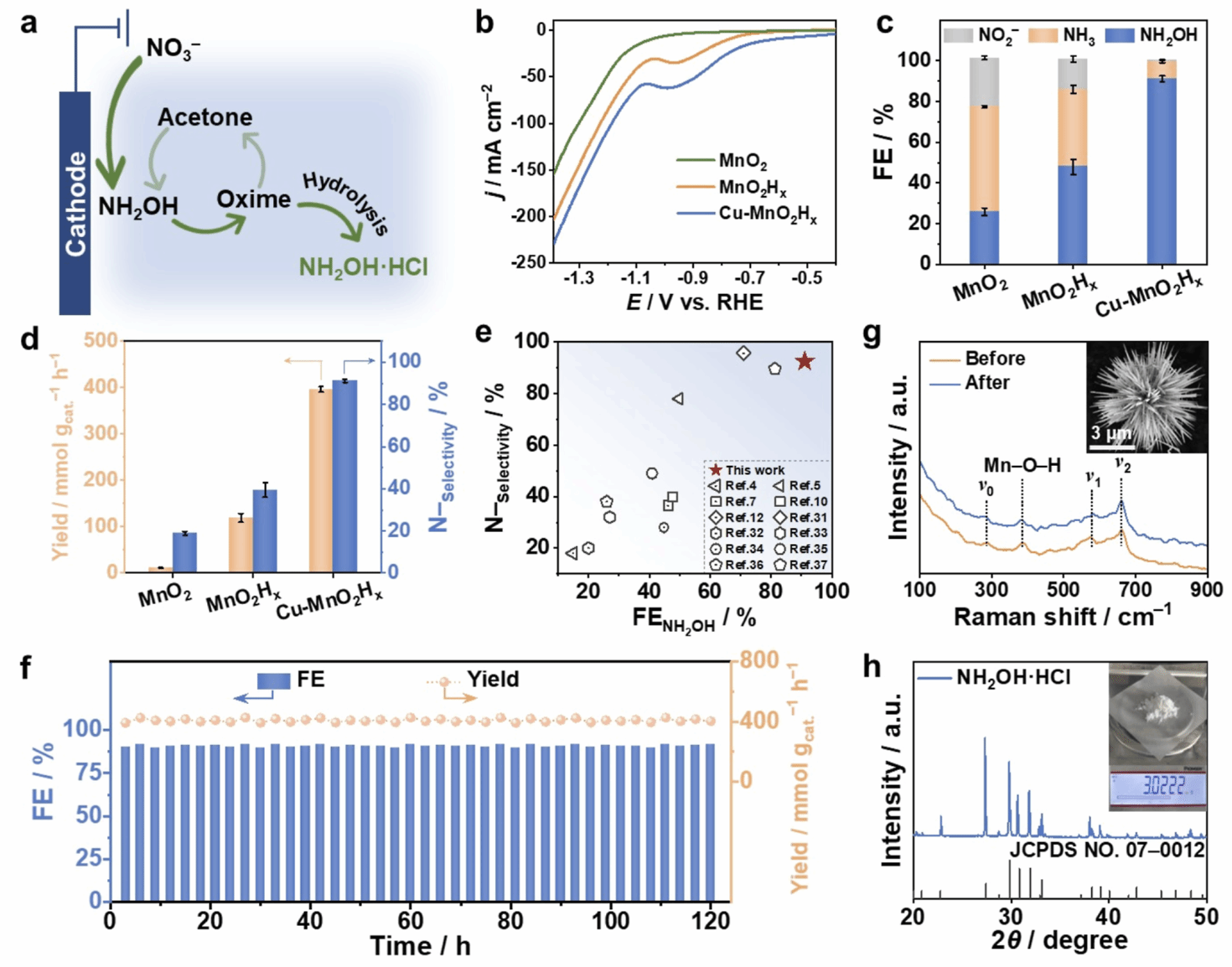
Figure 3:催化性能对比与长期稳定性
Cu-MnO₂Hx在−1.0 V时表现出最高羟胺选择性和产率。
产物比例远优于对照组,几乎无副产物。
120小时连续反应仍保持高活性,结构无明显变化。
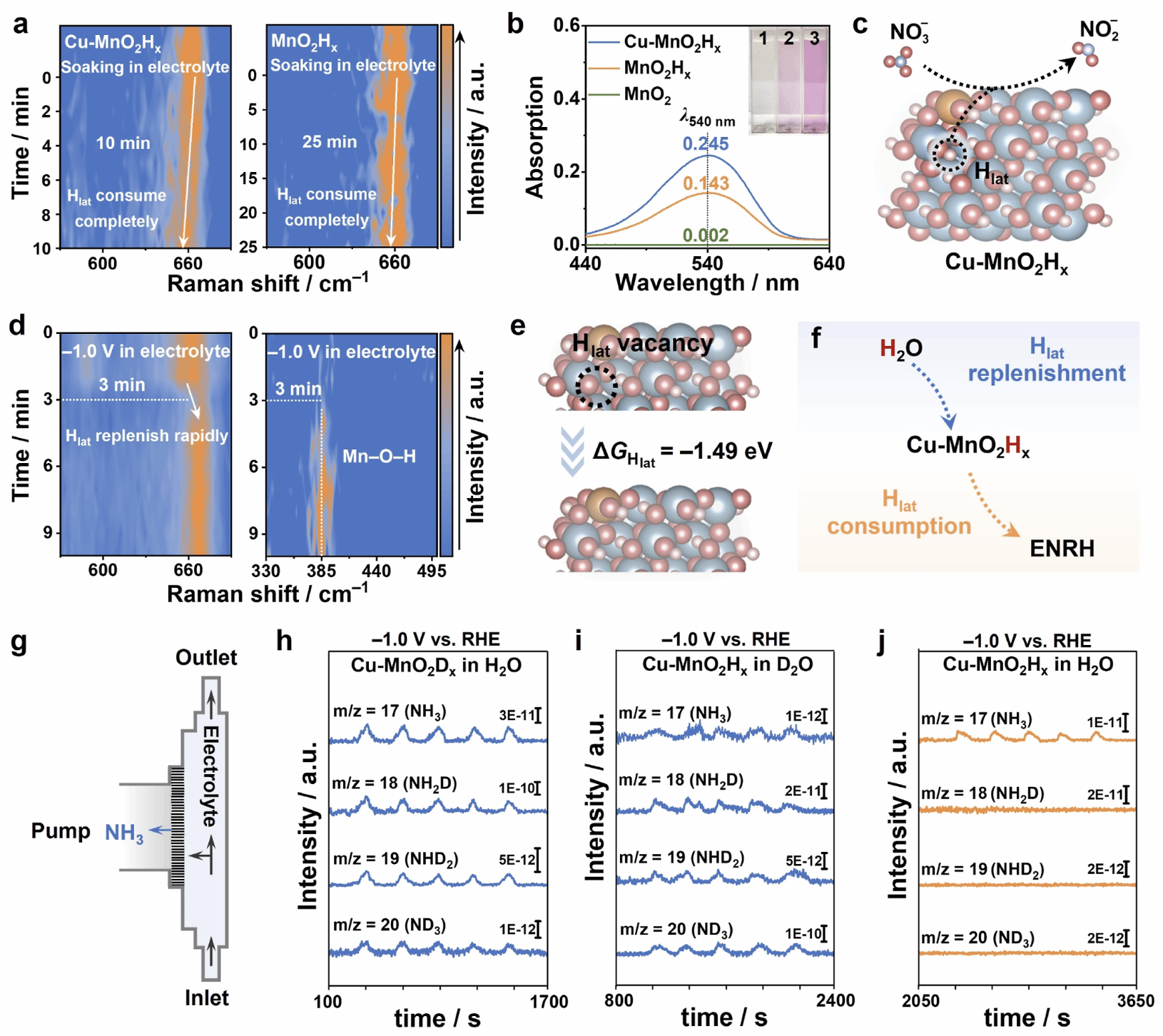
Figure 4:晶格氢的参与机制实证
原位Raman表明晶格氢可被NO₃⁻快速消耗。
同位素DEMS实验清晰证明晶格氢是羟胺的真实氢源。
晶格氢消耗后可通过水分解快速补充。
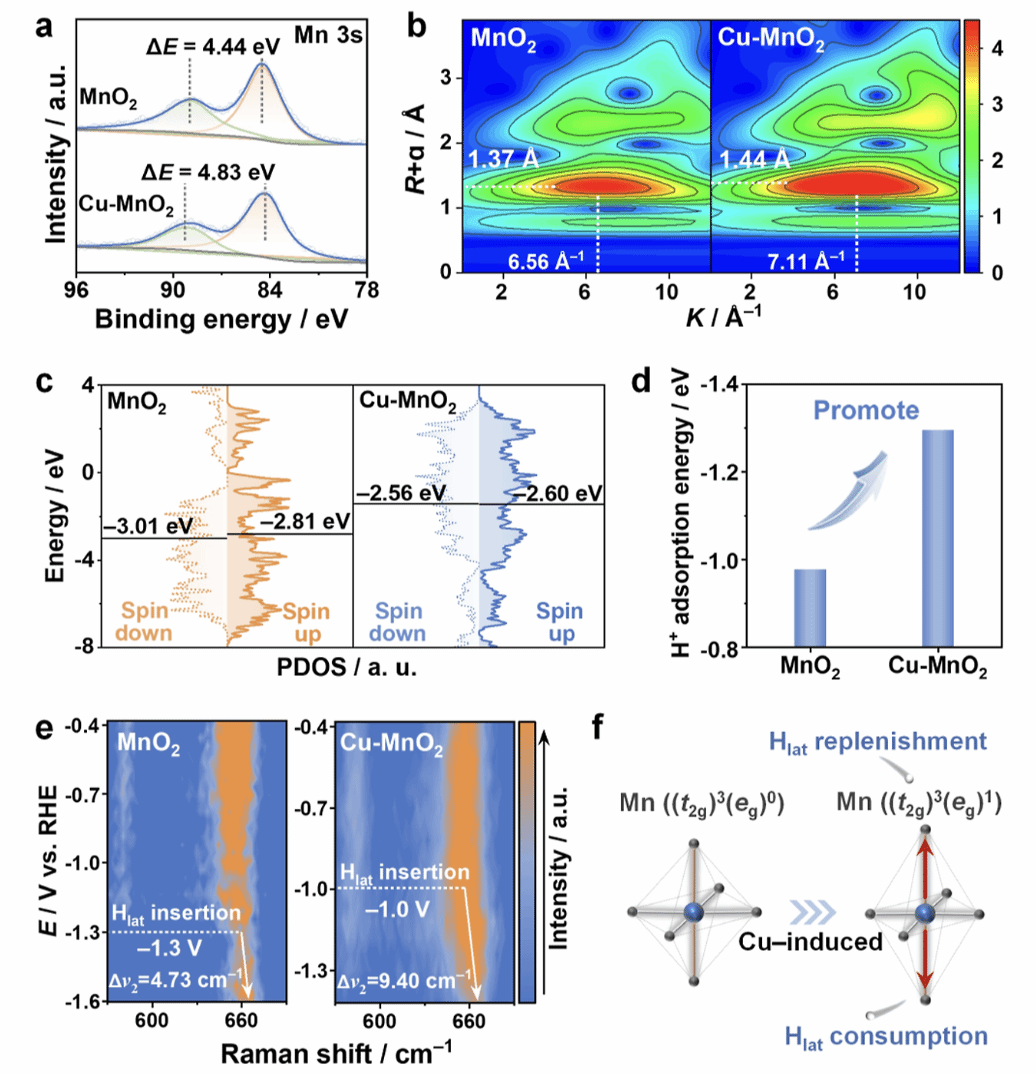
Figure 5:Cu增强晶格氢能力的本质机理
Cu掺杂诱导[MnO₆]八面体畸变,提升晶格氢储量。
PDOS分析表明O p带中心上移,有利于O–H键形成。
Cu-MnO₂Hx对晶格氢的吸附能更低,更利于生成与储存。
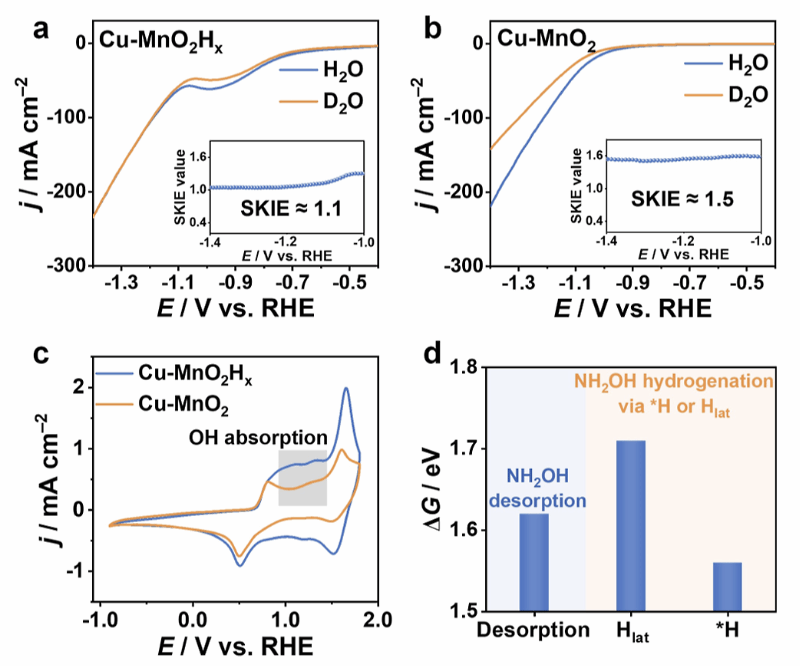
Figure 6:晶格氢的富集与缓冲效应机制
同位素效应表明Cu-MnO₂Hx的H来源更丰富。
晶格氢可提升*NH₂OH的解吸而非过还原,体现出“缓冲”作用。
“富集+缓冲”双功能使反应更高效且选择性更优。
文章总结
本研究以晶格氢为切入点,构建了具有高晶格氢储量与释放能力的Cu-MnO₂Hx催化剂,在电还原硝酸盐制羟胺反应中展现出优异性能。该策略有效解决了传统氢源在选择性与活性上的矛盾,为电催化还原反应提供了全新氢源调控路径。
启发与前景
🔹提供了一种普适性的“晶格氢参与”反应机制,可推广至其他电还原反应;
🔹Jahn-Teller调控策略为调控晶体结构与活性位提供新思路;
🔹有望推动羟胺等高附加值含氮化学品的绿色合成产业化进程。
文章来源:催化X公众号
DOI:10.1021/jacs.5c04863